MPGN bedeutet „membranoproliferative Glomerulonephritis“ und ist eine seltene Erkrankung des Nierenkörperchens (Glomerulus). Im Jahr 2010 wurde eine neue Klassifikation dieser einer Glomerulonephritis mit C3-Ablagerungen eingeführt, deren wesentliche Untergruppe die C3-Glomerulopathie (C3G) darstellt. [1]
Entsprechend den Ablagerungsmustern, die bei einer Nierenbiopsie festgestellt werden, kann C3G in weitere Untergruppen gegliedert werden [2]:
- membranoproliferative C3G,
- mesangiale C3G,
- membranöse C3G = dense deposit disease (häufig als DDD bezeichnet).
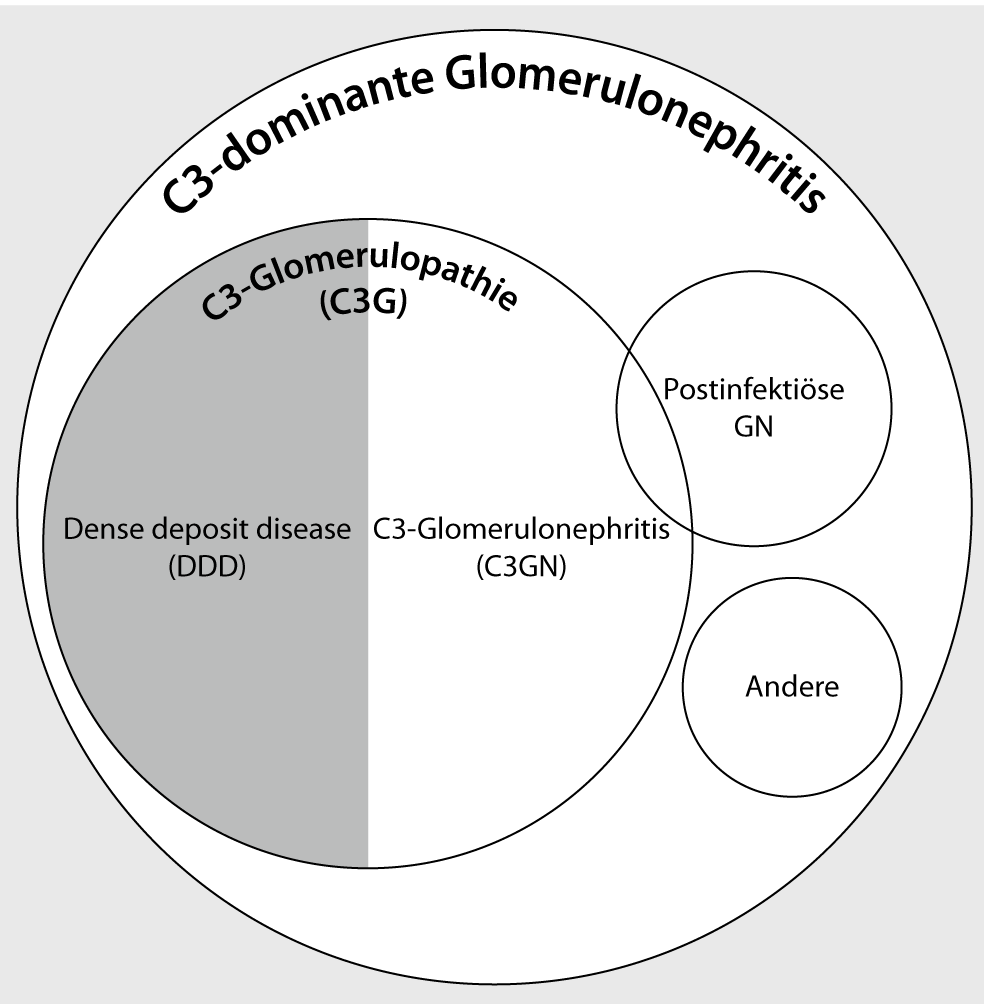
Findet sich bei Biopsie dagegen keine dominante Ablagerung von Komplement C3, sondern überwiegend von Immunglobulin G (IgG), ist von einer immunkomplexvermittelten, sog. sekundären MPGN auszugehen.
Symptome
- Proteinurie: Eiweiß im Urin – der Urin schäumt sich dabei; das Eiweiß kann durch Urinteststreifen oder mikroskopisch festgestellt werden;
- Hämaturie: bei Makrohämaturie ist die rosa oder rote Färbung des Urins mit bloßem Auge sichtbar; bei Mikrohämaturie kann das Blut durch Urinteststreifen oder mikroskopisch festgestellt werden;
- Ödeme – Schwellungen aufgrund einer Einlagerung von Flüssigkeit
- Hoher Blutdruck
Prognose
Ohne Behandlung führt C3G regelhaft zu einer progredienten Nierenfunktionsverschlechterung und endet innerhalb von 5 bis 10 Jahren in der Hälfte der Fälle mit einer terminalen Niereninsuffizienz (=Nierenversagen) [4]. Bei einer Nierentransplantation wird die neue Niere in den meisten Fällen nach einiger Zeit wieder angegriffen.
Ursachen [1]:
Die Hauptursachen der C3-Glomerulopathie sind Störungen des Komplementsystems, insbesondere des alternativen Komplementweges, welcher dadurch ständig übermäßig stark aktiviert wird. Die gestörte Regulation führt zur vermehrten Bildung und Aktivierung der C3-Konvertase oder/und der C5-Konvertase. Die Ursachen dafür können sein:
- der Ausfall einzelner oder mehrerer regulatorischer Komponenten, die für die Suppression des alternativen Komplementweges und damit für den Schutz der körpereigenen Zelloberflächen zuständig sind (z. B. Faktor H, CFHR1 an C3b und der C5-Konvertase und CFHR2 an der C3-Konvertase), oder
- die „Verfestigung“ der aktivierten C3- oder C5-Konvertase.
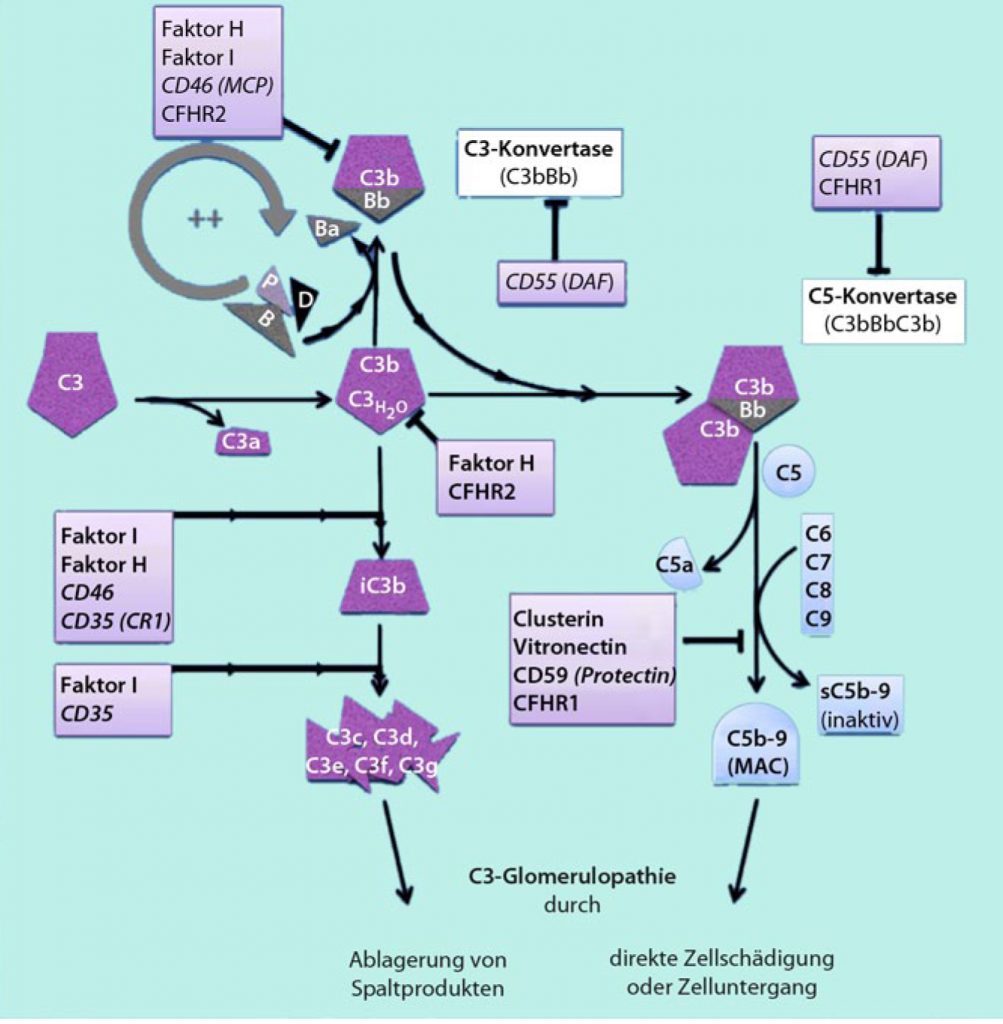
Verantwortlich dafür sind einerseits Mutationen im Bereich einzelner Komponenten, andererseits Autoantikörper, die zur Dysregulation des alternativen Komplementweges führen. Es gibt auch Fälle mit einem Mix aus Mutationen und Autoantikörpern wie auch mit einem Mix verschiedener Autoantikörper bei einem Patienten. Im Gegensatz zum atypischen hämolytisch-urämischen Syndrom (aHUS), bei dem ebenfalls eine Dysregulation des alternativen Komplementweges vorliegt, handelt es sich bei der C3G vermutlich primär um eine Komplementstörung in der Flüssigphase [3].
Folgen:
- Vermehrter Anfall biologisch aktiver C3- und C5-Fragmente (z. B. C3a, iC3b, C5a), die als Ablagerungen in der Niere gefunden werden und die Nierenerkrankung auslösen,
sowie - vermehrte Aktivierung des terminalen Komplementweges mit Produktion des C5b-9-Komplexes [1]. Der C5b-9-Komplex ist auch als Membranangriffskomplex (MAK, MAC) bekannt und bewirkt in der Zielzelle deren Tod. Bei aHUS und C3G greift er leider körpereigene Zellen an.
Diagnosestellung [1]:
- Nierenbiopsie: Entnahme des Nierengewebes (Glomeruli) und seine histopathologische Untersuchung durch Lichtmikroskopie und Elektronenmikroskopie
- Blutuntersuchungen: Bestimmung der C3- und C4-Werte
- Analytik des Komplementsystems: Bestimmung der Aktivierung des Komplementsystems und der Menge von C5b-9-Komplexen
- Nachweis von Autoantikörpern z. B. C3NeF, Anti-Faktor B, Anti-C3-Konvertase, Anti-Faktor-H
- Genetische Analyse: Mutationsanalyse von Faktor H, Faktor I, CFHR1-CFHR5 u.a.
Aufgrund der Seltenheit dieser Krankheitsbilder ist die Erfassung von Patienten in einem Register sehr wichtig, um möglichst bald eine verlässliche Behandlung zu finden. Über ein neues Register in Deutschland berichten wir in unserem Artikel The CompCure Study: Prospektive Kohortenstudie bei C3 Glomerulopathie.
Therapie
Für C3-Glomerulopathie gibt es seit April 2025 ein zugelassenes Medikament für Erwachsene ab 18 Jahren: Iptacopan (Handelsname Fabhalta). Es sind Kapseln, die zwei Mal täglich eingenommen werden müssen. Laut der Europäischen Arzneimittelbehörde (EMA) haben Studien der klinischen Phase III an 74 C3G-Patienten die Wirkung von Iptacopan belegt: Nach 6 Monaten Behandlung hat sich die Proteinurie bei den Probanden im Vergleich zur Placebo-Gruppe im Schnitt um 35 % reduziert. Die aktive Substanz in Iptacopan blockiert Faktor B – ein Protein im angeborenen Immunsystem (Komplementsystem) – und verhindert dadurch die Beschädigung von Nierenzellen. Zu den Nebenwirkungen gehören häufigere Atemwegsinfekte (bei >1 von 10 Patienten) und Pneumokokken-Infektionen (bei >1 von 10 Patienten). Außerdem besteht ein höheres Risiko im Vergleich zur Gesamtbevölkerung, an bekapselten Bakterien (Neisseria meningitidis, Streptococcus pneumoniae und Haemophilus influenzae Typ B) zu erkranken, weshalb die Abgabe des Medikaments nur an Patienten zugelassen ist, die gegen diese Erkrankungen geimpft sind. Mehr dazu können Sie der Webseite der Europäischen Arzneimittelbehörde (EMA) entnehmen: Link
Patienten ab 16 können an klinischen Studien der Phase III mit Iptacopan (Handelsname Fabhalta) teilnehmen. Mehr dazu finden Sie auf der Seite des Herstellers: Link
Für IC-MPGN wird demnächst (Stand Oktober 2025) die Zulassung von Pegcetacoplan (Handelsname Aspaveli) erwartet, das in den USA aufgrund der überragenden Daten aus klinischen Studien vorzeitig bereits im August 2025 für C3-Glomerulopathie und IC-MPGN für Patienten ab 12 Jahren zugelassen wurde. Bis dahin besteht die Möglichkeit, Pegcetacoplan außerhalb der Zulassung bei der zuständigen Krankenkasse zu beantragen, da das Medikament bereits seit 2023 für PNH zugelassen und auf dem Markt verfügbar ist.
Ansonsten gibt es nur eine Reihe therapeutischer Ansätze [1]:
1. Plasmaaustausch (PE) ermöglicht eine Elimination möglichweiser dysfunktionaler Komplementkomponenten oder pathogenetischer Antikörper: Diese Therapie führt in einigen Fällen zu einem partiellen therapeutischen Ansprechen.
2. Die Anwendung von Rituximab erbrachte bisher konträre Resultate.
3. Eculizumab (=Soliris® – das erste Mittel bei aHUS) bewirkt manchmal wesentliche Besserung des klinischen Zustands und der Nierenfunktion und führt in einigen Fällen zu einer Remission. Ein früher Therapiebeginn ist vermutlich mit einem besseren Ansprechen assoziiert.
4. Über weitere Medikamente, die gerade entwickelt werden und zu denen auch schon klinische Studien in Europa stattfinden, finden Sie Informationen auf unserer Seite “Studien zu MPGN/C§-Glomerulopathie”.
Diese und viele andere Informationen können Sie sich in den Videoaufnahmen und Vortragsfolien unserer Patiententage finden. Kontaktieren Sie hierfür bitte mpgn(at)ahus-selbsthilfe.de.
Wenn Sie der Forschung helfen möchten, diese Erkrankungen zu verstehen und neue wirksame Therapien zu entwickeln, können Sie Ihre Blutprobe anonymisiert in eine Datenbank einsenden lassen. Die Untersuchung ist kostenlos und im Fall von Auffälligkeiten werden Sie über Ihren Arzt darüber informiert. Mehr dazu finden Sie hier.
Weitere Informationen zur C3-Glomerulopathie
Auf unserer Website finden Sie Informationen zu
C3-Glomerulopathie und Umgang mit seltenen Krankheiten ist das Thema der 12. Folge im Podcast FuntioNIEREN: Link zum Podcast
Wir verfolgen für Sie außerdem internationale Fachkonferenzen. Im Oktober 2021 fand eine virtuelle Vorlesungsreihe der C3G-Experten aus Iowa (USA) statt. Die Vorträge in englischer Sprache finden Sie hier. Die Zusammenfassung in Deutsch können Sie als PDF-Datei herunterladen.
Hier sind die Themen der Vorträge:
Vortrag 1: Grundlagen des Komplementensystems, Diagnose C3-Glomerulopathie (Dr. Richard Smith) – Link zum englischsprachigen Video
Vortag 2: Wie wird C3-Glomerulopathie (MPGN Typ 2) behandelt und welche Medikamente werden entwickelt (Dr. Carla Nester) – Link zum englischsprachigen Video
Vortrag 3: Transplantationen und C3-Glomerulopathie (Dr. Christie Thomas) – Link zum englischsprachigen Video
Weitere Quellen für Betroffene:
https://kidneeds.lab.uiowa.edu/patients-and-families
Austausch mit anderen Betroffenen:
In deutscher Sprache: Facebook-Gruppe MPGN/C3G/DDD in Deutschland oder per E-Mail: mpgn(at)gmx.de
In englischer Sprache: eine sehr lebendige und weltweit vernetzte Facebook-Gruppe C3GN/DDD Warriors
Literatur:
[1] B. Hohenstein et al (2015): „State-of-the-art“: C3-Glomerulopathie und membranoproliferative Glomerulonephritis, Nephrologe 2015, 10:327–340
[2] Cook HT, Pickering MC (2015) Histopathology of MPGN and C3 glomerulopathies. Nat Rev Nephrol 2011:14–22
[3] Sethi S, Gamez JD, Vrana JA et al (2009) Glomeruli of dense deposit disease contain components of the alternative and terminal complement pathway. Kidney Int 75:952–960
[4] Medjeral-Thomas et al (2014) C3 glomerulopathy: clinicopathologic features and predictors of outcome. Clin J Am Soc Nephrol 9:46–53
